
Enant turşusu
Enant turşusu (heptan turşusu ) СH3(CH2)5СООН - birəsaslı doymuş karbon turşusudur. Bu yağlıtəhər rəngsiz maye xoşagəlməz qoxumuş yağ iyinə malikdir. Enant turşusunun duzları və anionları enantatlar adlanır. Enant turşusu suda az, lakin etanolda yaxşı həll olur.
== İzomerləri ==
Enant turşusunun aşağıdakı izomerləri var:
n-heptan turşusu СН3-СН2-СН2-СН2-СН2-СН2-COOH
5-metilheksanturşusu СН3-СН(СН3)-СН2-СН2-СН2-COOH
4-metilheksanturşusu СН3-СН2-СН(СН3)-СН2-СН2-COOH
3-metilheksanturşusu СН3-СН2-СН2-СН(СН3)-СН2-COOH
2- metilheksanturşusu СН3-СН2-СН2-СН2-СН(СН3)-COOH
3-etilpententurşusu СН3-СН2-СН(СН2-СН3)-СН2-COOH
2-etilpententurşusu СН3-СН2-СН2-СН(СН2-СН3)-COOH
== Mənbə ==
Merck Index, 11th Edition, 4581
David J. Anneken, Sabine Both, Ralf Christoph, Georg Fieg, Udo Steinberner, Alfred Westfechtel "Fatty Acids" in Ullmann's Encyclopedia of Industrial Chemistry 2006, Wiley-VCH, Weinheim.

Etilendiamintetrasirkə turşusu
Etilendiamintetrasirkə turşusu - Azərbaycan dilində qısaldılmış formada EDTS, ingilis dilində isə EDTA və bundan sonra –orjinalda olduğu EDTA kimi istifadə olunacaq,kimyəvi formulu (HOOCCH2)2N(CH2)2N(CH2COOH)2 – ibarət
dördəsaslı karbon turşusudur, ağ rəngdə kiçik kristallara malik tozdur, suda az həll olur, bütün üzvi həlledicilərdə həll olur, qələvilərdə həll olur, metal kationları ilə etilendiamintetraasetat duzlarını əmələ gətirir. O, etilendiaminin monoxlorsirkə turşusu ilə kondensasiyasından alınır.
== Tətbiqi ==
EDTA ikilinatriumduzlarının dihidratları (komplekson ııı, trilon B, Na2-ЭДТА) şəklində toxuculuq, dəri, kağız, lakboya sənayesində, metal, kauçuk istehsalında, kinematoqrafiyada, suyun yumşaldılmasında istifadə olunur. Analitik kimyada ETDA-dan istifadə etməklə 60-dan çox elementi təyin etmək mümkün olur. Təbabətdə ETDA-dan orqanizmdə olan zəhərli və radioaktiv metalları çıxarmaq üçün, qanın konservləşdirilməsi üçün istifadə olunur. EDTA kobalt duzu toksikologiyada sinil və ya xlorsianla zəhərlənmə zamanı antidot qismində istifadə olunur. Stomatologiyada diş kanallarını endodontik emalında istifadə olunur. EDTA farmaseptik texnologiyalarda selikli qişa vasitəsilə orqanizmə daxilolmanı gücləndirən komponent kimi istifadə olunur1.
Həmçinin kənd təsərrüfatında gübrə kimi istifadə olunur (elementlərin xelat formasında). Qidalandırıcı elementlərin xelat forması istər köklər və istərsə də yarpaqlar vasitəsilə yaxşı mənimsənilir.

Fenilsirkə turşusu
Fenilsirkə turşusu (α- toluol turşusu)- kimyəvi formulu С6H5СH2COOH olan üzvü birləşmədir.
== Fiziki xassələr ==
Fenilsirkə turşusu – parıltılı iynələrə bənzər, bal iyli bir maddədir. Üzvü birləşmələrdə həmçinin dietil efirində və etil spirtində yaxşı həl olunur.
Suda pis həl olunur 1,66 q/100 q (20 °C).
== Alınması ==
Fenilsirkə turşusunun sintezinin əksəriyyəti benzil - hallogenlərdən əmələ gəlir.
Fenilsirkə turşusu benzil nitrilin hidrolizi ilə sintez edilə bilər, öz növbəsində benzil bromidin natrium siyanidlə qarşılıqlı təsiri ilə əldə edə bilərik.
Fenilsirkə turşusunun ikinci sintez üsulu - benzilxloridin maqniumlaqarşılıqla təsirindən və sonradan alınan Qrinyar reaktivının karbon turşusu ilə reaksiyası nəticəsində alınır
PhCH2Cl + Mg
→
{\displaystyle \to }
PhCH2MgCl
PhCH2MgCl + CO2
→
{\displaystyle \to }
PhCH2COOMgCl
PhCH2COOMgCl + H2O
→
{\displaystyle \to }
PhCH2COOH + Mg(OH)Cl
== Tətbiqi ==
Fenilsirkə turşusu və efirləri ətir kompozisiyalarının və qida sirkəsinin hazırlanmasında istifadə olunur
Fenilsirkə turşusu amfetaminin sintezində bir başlanğıc maddə kimi istifadə olunur.
== Toksikliyi ==
Dovşanlar üçün fenilsirkə turşusunun yarım öldürücü dozası 5 q / kq təşkil edir.
== Mənbə ==
Рабинович В. А., Хавин З. Я. Краткий химический справочник. — Л.: Химия, 1977.
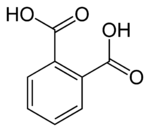
Ftal turşusu
Ftal turşusu' — (1,2-benzoldikarbon turşusu, ortoftal turşusu olaraq da bilinir[8]) — üzvi maddədir;iki əsaslı aromatik karbotsiklik turşuların ən sadə nümayəndəsidir. Onun duzlarına və efirlərinə ftalatlar deyilir. Tereftal və izoftal turşularının izomeridir. İysiz, rəngsiz monokristaldır.
== Tarixi ==
Ftal turşusu ilk dəfə 1836-cı ildə fransız kimyaçısı Auguste Laurent tərəfindən alınmışdır[4]. O,
naftalin tetraxloridi oksidləşdirərək ortoftal turşusunu əldə edib. Əldə etdiyi maddənin naftalinin törəməsi olduğunu zənn edərək, ona "naftalin turşusu"demişdir.[4][5] [ İsveçrəli kimyaçı Jean Charles Galissard de Marignac düzgün formulunu təyin etdikdən sonra,[6] Laurent indiki adını verdi. .[4][7 XIX əsrdə istehsal üsulları, naftalin tetraxloridinin nitrat turşusu ilə oksidləşməsini və ya daha yaxşı olaraq, katalizator kimi civə və ya civə (II) sulfatdan istifadə edərək, dumanlanan sulfat turşusu ilə karbohidrogenin oksidləşməsini əhatə edirdi. .[4]
== Alınması ==
Ftal turşusu kommersiya baxımından əhəmiyyətli bir məhsul deyil. Ftal anhidrid istehsalıbnda yan məhsul olaraq əmələ gəlir[9].

Gavalı turşusu
== Hazırlanma qaydası 1 ==
1 balon gavalı turşusunun hazırlanma qaydası:
== Tərkibi ==
2 kq gavalı
2x.q.duz
2x.q. üzüm sirkəsi
1ç.q. tünd sirkə (esensiya)
3 diş sarımsaq
1/2 ç.q. nanə qurusu
3 yarpaq dəfnə yarpağı
1 orta böyüklükdə acı bibər
5-6 ədəd qara istiot
== Hazırlanma qaydası ==
Sterilləşdirilmiş 3 litrlik balona sarımsaq, nanə qurusu, acı bibər, qara istiot və dəfnə yarpağı yığılır.Üzərinə yuyulmuş və çəngəllə deşilmiş gavalılar yığılır. Duz, esensiya və üzüm sirkəsi əlavə edilir və qaynar su tökülür. Ağzı ehmalca bağlanılır və soyumasını gözləyirik. Soyumuş məhlul ehmalca boşaldılır və yenidən qaynadılır. Gavalılar təkrar balona tökülərək germetik yolla qapaqla bağlanılır. Bağlanmış balon ağzı üstə çevrilir və soyuyana qədər saxlanılır.
== Hazırlanma qaydası 2 ==
== Tərkibi ==
Gavalı
Dəfnə yarpağı
Sarımsaq
Ətirli istiot
Duz
Esensiya (70% sirkə)
== Hazırlanma qaydası ==
Gavalını yuyub çəngəllə deşin, sarımsağı təmizləyin dilimlərə, istiotu və dəfnə yarpağını yuyun.

Hialuron turşusu
Hialuron turşusu (hialuronat, hialuronan) — birləşdirici, epitelial və sinir toxumalarının bir hissəsi olan sulfonlaşdırılmamış qlikozaminoqlikan. Bir çox bioloji mayelərin (tüpürcək, sinovial maye və s.) tərkibində olan hüceyrədənkənar matrisin əsas komponentlərindən biri. Hüceyrələrin çoxalmasında və miqrasiyasında mühüm rol oynayır.
Bu maddəyə "hialuron turşusu" adı 1934-cü ildə alman alimi Karl Meyer və J.V. Palmer tərəfindən verilmişdir.
Bəzi bakteriyalar (məs. Streptokokkus) tərəfindən istehsal olunur. Hialuron turşusu həmçinin A qrupunun streptokok ekstrasellüler kapsulunun tərkib hissəsidir və virulentlikdə rol oynadığı güman edilir.
70 kq olan insanın orqanizmində orta hesabla təxminən 15 qr. hialuron turşusu var və onun üçdə bir hissəsi hər gün dəyişir (parçalanır və ya sintez olunur).
== Funksiyaları ==
Hialuron turşusu sinovial mayenin özlülüyünə görə məsuliyyət daşıyan əsas komponentidir.
Hidroheksaflüorizoyağ turşusu
α-Hidroheksaflüorizoyağ turşusu (2-triflüormetil-3,3,3-triflüorpropion t-su, α- hidroperflüorizoyağ t-su)-(CF3)2CHCOOH, rəngsiz hiqroskopik kristal maddədir;
== Fiziki xassələri ==
Kəskin iyli, efirdə, asetonda və dioksanda yaxşı, suda isə pis həll olur (pKa — 2,35).
== Kimyəvi xassələri ==
α-Hidroheksaflüorizoyağ turşusunu P2O5-in köməyi ilə dehidratlaşdırdıqda davamlı bis-(triflüormetil)keten (CF3)2C=C=O, (C2H5)3N-in iştirakında dekarboksilləşdirdikdə isə 1,1,1,3,3,3-heksaflüorpropan (CF3)2CH2 alınır. α-Hidroheksaflüorizoyağın kalium duzu ~800C temperaturda 1,1,3,3,3-pentaflüorpropana CF3CH=CF2 çevrilir. α-H.t.-nin efirlərini dehidroflüorlaşdırdıqda perflüormetakril turşusunun efirləri CF2=C(CF3)COOR alınır.
== Alınması ==
α-H.t.-ni perflüorizobutileni (CF3)2C=CF2 üzvi həlledicilərdə hidratlaşdırmaqla alırlar.
== Tətbiqi ==
Laboratoriyada efirlərin və (CF3)2C=C=O-nun sintezində istifadə olunur.
== Mənbə ==
Химическая энциклопедия, Изд. "Советская энциклопедия", М., 1988, т. 1, с. 1085.

Həftəbecər turşusu
== Ərzaqlar ==
2 litrlik banka üçün
500 qr badımcan (təxminən 3 ədəd) — kiçik kublara doğranmış
1 kq (1 orta boy) kələm — yarı bölünüb nazik-nazik doğranmış
250 qr (2 ədəd) yaşıl bibər — iri-iri doğranmış
1 acı bibır (əgər turşunuzun bir az acı olmasını istəyirsinizsə istifadə edin) — iri-iri doğranmış
500 qr (4 ədəd) göy pomidor — iri-iri doğranmış
500 qr (4 ədəd) yerkökü — uzunsov nazik-nazik doğranmış (digər tərəvəzlər kimi də doğraya da bilərsiniz)
1 kərəvizin sapı — iri-iri doğranmış
1 baş sarımsaq — doğranmış
1 stəkan xırda doğranmış nanə
1 stəkan xırda doğranmış cəfəri
4 xörək qaşığı duz
təxminən 300 ml (1/3 litr) və ya bankanı dolduracaq qədər sirkə
== Hazırlanma qaydası ==
1. Doğranmış badımcanı aşsüzənə yığın və üstünə təxminən 2 xörək qaşığı duz səpin. Üzərinə ağırlıq (qapaq və ya qab) qoyun və 20 dəqiqə müddətində kənarda saxlayın. Sonra badımcanları yuyun, yaxşıca süzün, suyunu sıxın və qalın salfet və ya kağız dəsmalla qurulayın.
2. Doğradığınız bütün tərəvəz və göyərtiləri iri ləyənə qoyun. Üstünə 2 xörək qaşığı duz səpin və əlinizlə ərzaqları yaxşıca qarışdırın. 20 dəqiqə müddətinə kənara qoyun. Bu müddət ərzində tərəvəzlər sulanacaq.
3.

Kapril turşusu
Kapril turşusu (Oktan turşusu) С7Н15COOH - birəsaslı doymuş karbon turşusudur, yağlıtəhər rəngsiz, xoşagəlməz iyli, soyuqda kristallaşan mayedir.
== Təbiətdə tapılması ==
Kapril turşusu qliserid şəklində inək yağın tərkibində olur; Limburq pendirində, sivuş yağında (izoamil efiri şəklində) və çuğundur bəkməzində tapılmışdır; bitki yağlarından kokos yağının (6-10%), babassu palma yağının (2-8%), tukuma palma yağının (Astrocaryum vulgare) (1,3%), murumuru palma yağının (Astrocaryum murumuru) (1,1%), palma yağının (0,1%-dən az) tərkibidə vardır [2].
== Alınması ==
Olein turşusunun quru qovulması və normal oktil spirtinin oksidləşməsi zamanı əmələ gəlir.
== Mənbə ==
Solubility of octanoic acid in methanol
Растительные масла, в которых содержится каприловая кислота [1].

Kaprin turşusu
Kaprin turşusu (və ya dekan turşusu) CH3(CH2)8COOH – birəsaslı doymuş karbon turşusudur. Kaprin turşusunun duzları və anionları kaprinatlar adlandırılır.
== Təbiətdə tapılması ==
Kaprin turşusu inək yağının tərkibində, həmçinin bitki yağlarının: babassu yağının (7%), kokos yağının (5–10%), palma çəyirdəyi yağında (3–7%), gavalı tumunun yağında (4%), murumuru palma (Astrocarium murumuru) yağının (1,6%), tukuma palma (Astrocarium vulgare) yağının (1,6%), palma yağında (0,1% dən az)[1], az miqdarda spermaseti piyində rast gəlinir.
== Xassələri ==
Ağ rəngli kristallik maddə olub, otaq temperaturunda demək olar ki, suda həll olmur, qaynama temperaturu 268–270 °C, ərimə temperaturu 27–32 °C, sıxlığı isə 0,893 1/ml (25oC-də)-dir.

Kapron turşusu
Kapron turşusu (heksan turşusu) CH3(CH2)4СООН — birəsaslı doymuş karbon turşusudur. Kapron turşusunun duz və anionları kapronatlar adlanır.
== İzomerləri ==
Kapron turşusu ilə yanaşı, ümumi formulu С5Н11COOH olan 8 struktur izomeri də mövcuddur:
4-metilpentan turşusu СН3-СН(СН3)-СН2-СН2-COOH
3-metilpentan turşusu СН3-СН2-СН(СН3)-СН2-COOH
2 — metilpentan turşusu СН3-СН2-СН2-СН(СН3)-COOH
2-etilbutan turşusu СН3-СН2-СН(СН2-СН3)-COOH
3 — etilbutan turşusu СН3-СН(СН2-СН3)-СН2-COOH
3,3-dimetilbutan turşusu СН3-С(СН3)2-СН2-COOH
2,2 — dimetilbutan turşusu СН3-СН2-С(СН3)2-COOH
2,3 — dimetilbutan turşusu СН3-CH(СН3)-CH(СН3)-COOH
və 5 siniflərarası izomerlər:
Kapron turşusunun metil efiri СН3-СН2-СН2-СН2-COOH-СН3
Kapron turşusunun etil efiri СН3-СН2-СН2-COOH-СН2-СН3
Kapron turşusunun propil efiri СН3-СН2-COOH-СН2-СН2-СН3
Kapron turşusunun butil efiri СН3-COOH-СН2-СН2-СН2-СН3
Kapron turşusunun pentil efiri COOH-СН2-СН2-СН2-СН2-СН3
== Fiziki xassələri ==
Kapron turşusu – xoşagəlməz iyli, rəngsiz, yağlı mayedir. Suda pis həll olur (9.68 q/l (20°С), 11.71 q/l (60°С). Metanol, etanol, efirdə yaxşı həll olur.
== Kimyəvi xassələri ==
Kimyəvi xassələrinə görə kapron turşusu doymuş alifatik karbon turşularının tipik nümayəndəsidir. Orta qüvvətli turşudur (pKa 4.88). Ondan duzlar və mürəkkəb efirlər, halogenanhidridlər və anhidridlər alınır. Kapron turşularının duz və efirləri heksanatlar adlanır. Bromla fosforun iştirakı ilə α-vəziyyətdə bromlaşır.

Karbonat turşusu
Karbonat turşusu — kimyəvi formulu H2CO3 olan zəif ikiəsaslı turşu. Turşuların bütün xassələrinə malikdir.
Karbonat turşusu normal şəraitdə suya və karbon qazına parçalandığına görə sərbəst halda mövcud deyil:
CO2 + H2O ↔ H2CO3
Karbonat turşusunun molekulundakı kimyəvi rabitə polyar kovalent rabitələrdir.
== Karbonat turşusunun törəmələri ==
Karbonat turşusunun da başqa üzvi turşular kimi müvafiq törəmələri vardır. Bu törəmələrdən karbonat turşusunun xloranhidridlərini, esterlərini və amidlərini göstərmək olar.
== Karbonat turşusunun xloranhidridləri ==
Karbonat turşusunun iki cür xloranhidridi ola bilər. Bunalrada xlorkarbonat turşusu, ikincisi karboksixlorid və fosgen adlanır.
Fosgen və ya karboksixlorid birinci dəfə Devi tərəfindən dəm qazına günəz işiğının təsiri ilə xlor birləşdirməklə alınmışdır, buna görə də fosgen (fos-yunanca) işıq adlanmışdır. İndi, fosgen üçün dəm qazı ilə xloru 2000-də kömür katalizatoru üzərindən buraxılırlar.
Fosgen zəhərli boğucu qazdır, 80C-də qaynayır, benzolda yaxşı həll olur, su ilə parçalanır, karbon qazı ilə xlorid turşusu əmələ gətirir.

Kəhrəba turşusu
Kəhrəba turşusu (butandion turşusu, etan-1,2-dikarbon turşusu) – ikiəsaslı doymuş karbon turşusudur. Ağ rəngli kristallar olub, suda və spirtdə həll olur, butun bitkilərin tərkibində, kəhrəbada az miqdarda vardır. Bitkilərin boy artımını ctimullaşdırır və məhsuldarlığı artırır, qarğıdalının inkişaf etməsini sürətləndirir.
Ilk dəfə kəhrəba turşusunu XII əsrdə kəhrəbanın birbaşa qovulmasından almışlar.
Sənayedə isə kəhrəba turşusu, əsas etibarı ilə, malein anhidridinin hidrogenləşdirilməsindən alınır. Kəhrəba turşusunun duzu və efirləri suksinatlar (lat. Succinum – kəhrəba) aşlandırılır.
== Xassələri ==
=== Orqanoleptik xassələri ===
Kəhrəba turşusu ağ kristalar olub, zəif və yüngul duzlu-acıtəhər dada malikdir [2].
=== Fiziki xassələri ===
Ərimə temperaturu 183oC, qaynama temperaturu 235 oC-dir. 235oC-dən yuxarı temperaturda özündən Н2О ayırır və kəhrəba anhidridinə çevrilir.

Kələm turşusu
Kələm turşusu — bir çox mətbəxdə geniş istifadə olunan, kələmdən hazırlanan turşu növü. Əsasən qış aylarında daha çox istifadə olunur.
== Tarixi ==
Qədim Roma yazıçıları Böyük Katon və Kolumella əsərlərində kələm turşusundan bəhs etmişdirlər. Kapitan Ceyms Kuk səyahətləri zamanı özü ilə kələm turşusu ehtiyatları götürürdü.
== Yayılması ==
Kələm turşusu Şərqi Avropa ölkələrindən Azərbaycan, Rusiya, Belarus, Estoniya, Latviya, Litva, Moroviya, Polşa, Ukrayna mətbəxlərində geniş istifadə olunur. Rusiya mətbəxində bəzən piraşkinin içərisinə kələm turşusu qoyulur. Polşada biqos yeməyinin inqredientidir.
Almaniya və Avstriyada kələm turşusu giləmeyvələrlə dadlandırılır. Çilidə kələm turşusu hotdoq və sendviçlərdə istifadə olunur. Pensilvaniyada Yeni il ərəfində kələm turşusu yemək ənənəsi mövcuddur.

Limon turşusu
Limon turşusu (2-hidroksi-1,2,3-propantrikarbon turşusu, 3-hidroksi-3-karboksipentandiol) (C6H8O7) — ağ rəngli kristal maddədir; el arasında "lumu duzu" və ya "limon duzu" kimi da tanınır [1] Arxivləşdirilib 2016-04-09 at the Wayback Machine.
== Xassələri ==
Ərimə temperaturu 153 °S-dir. Suda yaxşı həll olur. Etil spirtində həll olur. Dietil spirtində az həll olur. Üçəsaslı zəif turşudur. Limonturşusunun duzları və efirləri sitratlar adlanır.
== Alınma qaydası ==
Limon turşusu limon və ya yabanı nar şirəsindən, eləcə də tənbəki yarpaqlaından, şəkər məhlulunu xüsusi göbələklərlə qıcqırtmaqla alınır. Qeyd edək ki, tütündə 7-8%, yabanı narda 9%, limonda isə 10%-ə qədər limon turşusu olur. Limon turşusunun limon və nar şirəsindən alınması çox mürəkkəb prosesidir.

Malein turşusu
Malein turşusu - HOOC-CH = CH-COOH formuluna malik ikiəsaslı doymamış üzvi birləşmədir. Beynəlxalq nomenklatura ilə adı sis-butenedio turşusudur. Onun trans izomerinə fumarin turşusu deyilir.Malein turşusunun duzlarına və efirlərinə maleatlar deyilir.Ən çox fumarin turşunun istehsalında istifadə olunur.
== Fiziki xassələri ==
Malein turşusu molekulu fumarin turşusundan daha az stabildir. Yanma istiliyi arasındakı fərq 22.7 kJ / mol təşkil edir [1].
Malein turşusu suda çox yaxşı həll olur (25 °C -də 78.8 q / l), fumarin turşusu zəif həll olur (25 °C -də 6.3 q / l). Bu xüsusiyyətlər malein turşusu molekulunda molekullararası hidrogen bağının əmələ gəlməsi ilə izah olunur.
== Tarıxi və alınma metodları ==
Malein turşusu ilk dəfə 1819 -cu ildə alma turşunun distillə edilməsi yolu ilə Lassen tərəfindən alınmışdır. Perkinə (1881) görə, onu əldə etmək üçün alma turşusu asetil xloridlə işlənir, sirkə-alma anhidridi əmələ gətirir, onun hidratlaşması nəticəsində malein turşusu əmələ gəlir.
Prosesin ümumi sxemi:
== Sənayedə istehsalı ==
Sənayedə malein turşusunu aşağıdakı sxemə görə benzolun katalitik oksidləşməsindən alınan malein anhidridinin hidrolizindən əldə edilir:
== Sənayedə tətbiqi ==
Malein turşusunun ən vacib istifadəsi fumarin turşunun istehsalındatətbiqidir.
Malon turşusu
Malon turşusu (propandion t-su, metandikarbon t-su)-rəngsiz kristal maddədir,
== Fiziki xassələri ==
Suda (100 qramda 73,5 q) və etanolda yaxşı həll olur, piridində və dietilefirində (5-10%) həll olur, benzolda həll olmur. Qələvi metallarla duzlar suda yaxşı həll olurlar, Ba və Pb-duzları isə həll olmur. Malon turşusunun duzları və efirləri malonatlar adlanır. Ca-duzu şəkər çuğundurunun şirəsində rast gəlinir.
== Kimyəvi xassələri ==
M.t. karboksil qruplarına görə iki sıra törəmələr əmələ gətirir (turş və tam); efirlər (məs., malon efiri), nitrillər (sian sirkə turşusu və malononitril), amidlər, xloranhidridlər. Məs., malon turşusunun SO2Cl2 ilə qarşılıqlı təsirindən reaksiyanın şəraitindən asılı olaraq tam xloranhidrid (malonilxlorid) ClCOCH2COCl və ya turş xloranhidrid ClCOCH2COOH alınır.
Ərimə t.-dan yuxarı t.-da və ya suda məhlulunu 700C-dən yuxarı qızdırdıqda M.t. asanlıqla dekarboksilləşərək sirkə turşusuna çevrilir. M.t.-nin əvəzediciləri də anoloji olaraq monokarbon turşularına çevrilirlər:
P2O5-lə qızdırdıqda M.t.

Metakrilat turşusu
Metakrilat turşusu (C4H6O2) — doymamış birəsaslı karbon turşusudur.
Kəskin iyli mayedir. Qatı rəngə malikdir. Suda yaxşı həll olur.
Metakrilat turşusunun kimyəvi xassələri Karbon turşusunun kimyəvi xassələrinin analoqudur, yəni, eynisidir. Metakrilat turşusu Polimerləşə bilir.
Metakrilat turşusundan polimetakrilat turşusu və mürəkkəb efirlərin sintezində istifadə edilir.

Mezoçaxır turşusu
Mezoçaxır turşusu- çaxır turşusunun izomeridir.
Mezoçaxır turşusu başqa çaxır turşularından da sabit turşudur. Bir molekul su ilə kristallaşır, susuz turşu halında 140C-də əriyir.
Mezoçaxır turşusu üzüm turşusu kimi optik qeyri-fəaldır, ancaq ondan fərqli olaraq sağ və sol antipodlara ayrıla ilmir.
d-çaxır turşusu təbiətdə rast gəlir və praktiki cəhətdən maxır turşularının ən əhəmiyyatlisidir. Bu turşu üzümdə və maxıra rast gəlir. Maxır hazırlanan qablarda spirtin miqdarının artması nəticəsində d-maxır turşusu turş kalium duzu şəklində KOOC-CHOH-CHOH-COOH kalium-hidroartarat və ya maxır daşı çökür. Bu duza mineral turşularla təsir etdikdə d-maxır turşusunu almaq olar, d-çaxır turşusu 1700C-də əriyir, suda cə spirtdə yaxşı həll olur. polyarizasiya olunmuş işıq müstəvisini sağa fırladır. Qatılığından asılı olaraq məhlulda onun fırlatma dərəcəsi dəyişir.

Monoxlorsirkə turşusu
Monoxlorsirkə turşusu CH2ClCOOH – metil qrupunun 1 hidrogen atomu Cl atomuna əvəz olunmuş sirkə turşusudur, rəngsiz kristallardır.
Tərimə = 61,20C, Tqayn.=189,30C. Suda, spirtdə, asetonda, efirdə həll olur.
Monoxlorsirkə turşusu – indiqo və başqa boyaların sintezində aralıq məhsuldur, karboksimetilsellülozanın, herbisidlərin (məsələn, 2,4-dixlorfenoksi sirkə turşusunun duzları və efirləri), B6 vitaminin alınmasında istifadə olunur.
Üzvi kimyada onun faydalığının illüstrasiyası (aydın nümunəsi) salisil aldehidinin xlorsirkə turşusu ilə O-alkilləşməsi, ardınca alınmış efirin dekarboksilləşməsi ilə benzofuranın alınmasıdır.
Reaksiyaların əksəriyyətində C-Cl rabitəsinin yüksək reaksiya qabiliyətindən istifadə edilir.
Herbisid olan qlifosat üçün prekursordur (yəni ondan əvvəl əmələ gələn). MXFST (2-metil-4-xlorfenoksi sirkə turşusu) herbisidi xlorsirkə turşusunun alkillləşməsi ilə alınmışdır. Xlorsirkə turşusunu xlorasetil xloridə, adrenalinin prekusoruna çevirirlər.
PVC stabilizatoru və bəzən kosmetikada komponent kimi istifadə edilən tioqlikol turşusu xlorun kükürdlə əvəzolunma reaksiyası ilə əldə edilir.
Əlavə məlumat: [PVC- neft və ya təbii qazdan alınan polimer növüdür.

Nikotin turşusu
Vitamin PP (B3) nikotin turşusu və ya niasin də deyilir. Vitamin B3 orqanizmə qida vasitəsilə daxil olur. Ətdə, böyrəkdə, xüsusilə, qaraciyər və bəzi bitkilərdə (düyü, buğda və s.) rast gəlinir. Orqanizmdə B3 vitamini triptofandan da alınır. Bu vitaminin sintezi aşağdakı reaksiya ilə alınır.
B3 vitamininə olan gündəlik təlabat 25 mq-dır. Vitamin B3 bir sıra kofermentlərin tərkibində olub aşağıdakı biokimyəvi reaksiyalarda iştirak edir:
Oksidləşmə-reduksiya reaksiyasında hidrogen daşınma funksiyasıni (NADH) yerinə yetirir;
Allosterik effektor kimi nizamlayıcı rolunu oynayır;
Sintetik reaksiyalarda substrat rolunu oynayır.
Orqanizmdə B3 vitamini çatmadıqda pellaqra xəstəliyi əmələ gəlir. Pellaqra sözü yunanca pelle və aqra sözündən götürülüb, mənaca dərinin kələ-kötürləşməsi deməkdir. Əlamətləri aşağıdakılardan ibarətdir: dəridə yara əmələ gəlir, həzm sisteminin funksiyası pozulur, əqlin zəif inkişaf etməsi və s.

Nitrat turşusu
Nitrat turşusu (HNO3) – birəsaslı, qüvvətli turşu.
Adi şəraitdə rəngsiz mayedir. Kimya sənayesinin ən mühüm məhsullarından biridir. Susuz Nitrat turşusunun sıxlığı 1,522 q/sm3-dir, —41°C-də donur, 86°C-də qaynayır. Su ilə istənilən nisbətdə qarışır və azeotrop qarıqiıq əmələ gətirir.
İki kristalhidratı məlumdur: HNO3·H2O və HNO3·3H2O. Susuz nitrat turşusu davamlı deyildir, adi temperaturda işıqda parçalanaraq oksigen çıxarır (4HNO3=4NO2-2H2O + O2). Nitrat turşusu qüvvətli oksidləşdiricidir, kükürdü sulfat turşusuna çevrilincəyə qədər oksidləşdirir, yalnız qızıla, tantala və platin fəsiləsinin bəzi metallarına təsir etmir. Metallarla reaksiyaya girib azot 2-oksid çıxarır. Durulaşdırılmış nitrat turşusunda asan həll olan bəzi metallar, məsələn, dəmir, xrom, alüminium, metalın səthində qoruyucu oksid təbəqəsi əmələ gətirdiyi üçün qatı nitrat turşusuna qarşı davamlıdır. Bu xüsusiyyət qatı nitrat turşusunu polad qablarda saxlamağa və daşımağa imkan verir.

Nitrit turşusu
Nitrit turşusu (HNO2) — zəif birəsaslı turşu.
Nitrit turşusu normal şəraitdə bərk halda olur. Nisbi molyar kütləsi 47,0134 а.k.v., molyar kütləsi isə 47.0134 q/mol-dur.
Türşü 42,35 °S-də əriyir və maye halda sıxlığı 1.685 q/sm³-dur. Nitrit turşusunun qaynama temperaturu 158 °S-dir.
2
HNO
2
⟷
N
2
O
3
+
H
2
O
⟷
NO
↑
+
NO
2
↑
+
H
2
O
{\displaystyle {\ce {2 HNO2 <-> N2O3 + H2O <-> NO ^ + NO2 ^ + H2O}}}
3
HNO
2
⟷
HNO
3
+
2
NO
↑
+
H
2
O
{\displaystyle {\ce {3 HNO2 <-> HNO3 + 2 NO ^ + H2O}}}
HNO2 zəif turşudur.
H
2
SO
4
+
2
NaNO
2
⟶
Na
2
SO
4
+
2
HNO
2
{\displaystyle {\ce {H2SO4 + 2 NaNO2 -> Na2SO4 + 2 HNO2}}}
HNO
2
+
H
2
O
2
⟶
HNO
3
+
H
2
O
{\displaystyle {\ce {HNO2 + H2O2 -> HNO3 + H2O}}}
HNO
2
+
Cl
2
+
H
2
O
⟶
HNO
3
+
2
HCl
{\displaystyle {\ce {HNO2 + Cl2 + H2O -> HNO3 + 2 HCl}}}
7
HNO
2
+
2
KMnO
4
⟶
2
Mn
(
NO
3
)
2
+
2
KNO
3
+
3
H
2
O
+
HNO
3
{\displaystyle {\ce {7 HNO2 + 2 KMnO4 -> 2 Mn(NO3)2 + 2 KNO3 + 3 H2O + HNO3}}}
2
HNO
2
+
2
HI
⟶
2
NO
↑
+
I
2
+
2
H
2
O
{\displaystyle {\ce {2 HNO2 + 2 HI -> 2 NO ^ + I2 + 2 H2O}}}
Nitrit turşusunu azot- 3 — oksidini H2O suda həll etməklə:
N
2
O
3
+
H
2
O
⟶
2
HNO
2
{\displaystyle {\ce {N2O3 + H2O -> 2 HNO2}}}
Nitrit turşusunu azot- 4 — oksidini H2O suda həll etməklə:
2
NO
2
+
H
2
O
⟶
HNO
3
+
HNO
2
{\displaystyle {\ce {2 NO2 + H2O -> HNO3 + HNO2}}}
Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия.

Oksalat turşusu
Oksalat turşusu (turşəng turşusu) – (etandion turşusu, kimyəvi formulu — C2H2O4 və ya HOOC-COOH) doymuş karboktsilik turşular sinfinə aid güclü kimyəvi üzvi turşudur.
Standart şəraitdə oksalat turşusu ağ kristal maddə olan iki əsaslı doymuş karbotksilik turşudur.
Oksalat turşusunun duzları və efirləri oksalatlar adlanır.
Oksalat turşusu ilk dəfə 1824-cü ildə alman kimyaçısı Fridrix Völer tərəfindən disiandan sintez edilmişdir.
Təbiətdə turşəng, rhubarb, karambola və bəzi digər bitkilərdə sərbəst formada və kalium və kalsium oksalatları şəklində olur.
Sənayedə oksalat turşusu karbohidratların, spirtlərin və qlikolların HNO3 və H2SO4 qarışığı ilə V2O5 iştirakında, və ya etilen və asetilenin HNO3 ilə PdCl2 və ya iştirakı ilə oksidləşməsi, həmçinin propilenin maye NO2 ilə oksidləşməsi ilə alırlar.
Turşəng turşusunun alınmasının perspektivli üsulu CO ilə NaOH-dan natrium formaitdan keçməklə alınmasıdır:
2HCOONa=NaOOC-COONa=HOOC-COOH(Oksalat turşusu)
2HOOC-COOH+ 2Na= 2HOOC-COONa+H²(turş duz)
HOOC-COOH+ 2NaOH= NaOOC-COONa+2H²O(Normal duz)
Onun həmçinin aşağı temperaturda turşu mühitində asetilendən alınması da tətbiq olunur:
5C2H2 + 8 KmnO4 + 12H2SO4 → 5 HOOC–COOH + 8MnSO4 + 4K2SO4 + 12H2O
Yanma entalpiyası (ΔH0yanma) −251,8 kJ/mol
Dekarboksilləşmə temperaturu 166–180 °C
Laboratoriyalarda oksalat turşusu hidrogen xlorid və hidrogen yodid almaq üçün istifadə olunur:
Oksalat turşusu həmçinin xlor dioksidin laboratoriya sintezi üçün də istifadə olunur:
Oksalat turşusu və oksalatlar toxuculuq və dəri sənayesində mordant kimi istifadə olunur. Onlar metal örtüklərin — alüminium, titan və qalayların çökməsi üçün anod vannalarının komponentləri kimi xidmət edirlər.
Oksalat turşusu və oksalatlar analitik və üzvi kimyada istifadə olunan reagentlərdir. Onlar metal üzərində pas və oksid örtüklərini çıxarmaq üçün kompozisiyalara daxildir; məhluldan nadir torpaq elementlərinin çökdürülməsi üçün istifadə olunur.

Oksisirkə turşusu
Oksisirkə turşusu — HOCH2-COOH, ikiatomlu oksiturşudu.. Bu turşu qlikolun ehtiyatlı oksidləşməsi nəticəsində alına bildiyi üçün qlikol turşusuda adlanır.
Qlikol turşusu qora suyunda və başqa kal meyvələrdə rast gəlinir. Qlikol turşusu bərk maddə olub, 79–80oC-də əriyir, suda asan həll olur.
M. Mövsümzadə, P. Qurbanov "Üzvi kimya", Maarif-1983.